在藥廠與生技製程中,空氣微生物監測(Environmental Monitoring, EM)並非單純的例行檢測,而是品質系統(Quality System)中的一個環節。
隨著 GMP 查核對資料完整性(Data Integrity)的要求日益嚴格,QA 在選擇空氣採樣設備時,關注的已不只是是否完成採樣,而是資料是否能被清楚說明、完整追溯,並可支撐稽核需求。
在此背景下,ALCOA+ 成為評估資料品質的重要原則。
ALCOA+ 強調資料必須具備可歸屬性(Attributable)、可讀性(Legible)、即時性(Contemporaneous)、原始性(Original)與準確性(Accurate),並進一步延伸至資料的一致性、完整性、耐久性與可取得性。
對 QA 而言,ALCOA+ 不只是查核標準,更是設備與流程設計時必須納入的基本思維。
TRIO.BAS 的空氣微生物採樣系統,正是以這樣的 QA 視角進行設計。
一、資料在產生當下即具備可追溯性
(Attributable / Contemporaneous / Legible)
ALCOA+ 的第一步,是確保資料在產生當下即具備可追溯性。
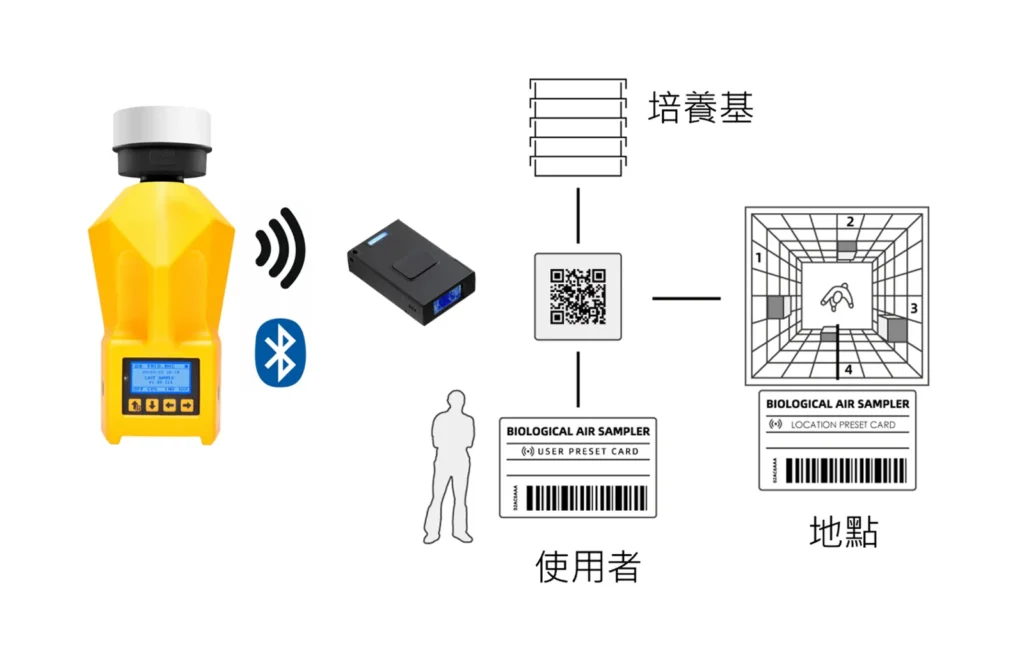
TRIO.BAS 每一次採樣,均可完整記錄並追溯以下資訊:
- 採樣時間
- 採樣地點
- 操作人員
- 採樣體積
- 使用的培養基
上述資訊與採樣結果一併保存,使 QA 能清楚說明該筆資料由誰、於何時、何地、在何種條件下產生。
此設計對應 Attributable、Legible 與 Contemporaneous 的實務要求。
二、區分哪些資料屬於 GMP,是資料完整性的起點
(Consistent / Complete)
在 GMP 環境中,並非所有操作都應成為正式監測資料。
TRIO.BAS 清楚區分兩種操作模式:
- 手動模式:無需密碼登入,適用於功能測試或非 GMP 操作
- 自動模式:需密碼登入,區分管理員與用戶,適用於正式環境監測
透過模式分流,QA 能明確界定哪些資料可納入 GMP 趨勢分析,哪些操作不屬於正式監測範疇。
避免不同性質的資料混用,是符合GMP資料一致性與完整性的關鍵。
三、以系統權限控管操作責任與資料存取
(Consistent / Available)
當資料被正確產生後,下一步關鍵在於操作與存取權限的控管。
TRIO.BAS 搭配 BAS SW電腦軟體,將採樣作業由單機操作提升為系統化管理,其設計包含:
- 密碼登入機制
- 三等級權限管理(高級權限、管理員、標準使用者)
- 使用者、採樣地點與採樣設定的集中管理
透過清楚的權限劃分,QA 能掌握誰可設定設備、誰可執行採樣、誰可存取或匯出資料,確保資料在整個流程中的一致性與可控性。
四、原始資料與輸出資料清楚區分
(Original / Accurate)
在資料完整性的實務查核中,原始資料的保存方式是常見重點。
TRIO.BAS 支援多種資料格式,包括:
- .bas(加密原始格式)
- PDF、CSV、XML(報告、分析與系統整合用途)
其中,.bas 檔案作為原始資料保存,其餘格式用於後續分析與應用。
此設計可協助 QA 清楚說明資料的原始性、準確性,以及資料從產生到使用的完整流程。
五、資料可被安全取得,同時符合內部控管需求
(Available)
TRIO.BAS 的資料可透過藍牙或有線方式傳輸至電腦系統。
使用單位可依內部 IT 或資訊安全政策,選擇合適的資料傳輸方式,在操作便利性與系統控管需求之間取得平衡,確保資料可取得且不失控。
六、從資料產生到保存,形成支援 Part 11 的完整閉環
(ALCOA+ 整體一致性)
透過上述設計,TRIO.BAS 在資料產生、分類、控管、保存與使用各階段,形成一致且可被查核的操作與資料管理架構。
此架構可支援 FDA 21 CFR Part 11 對電子紀錄與資料完整性的相關要求,使合規不僅體現在設備本身,也落實於日常操作流程中。
結論:以 QA 為核心,而非事後補救的空氣微生物監測系統 對 QA 而言,真正關鍵的不是設備功能多寡,而是資料是否清楚、可控、可追溯,並能在稽核時被合理說明。 TRIO.BAS 以 ALCOA+ 為設計核心,從採樣到資料輸出,協助企業建立一套可被信任、可長期運行的環境監測系統。 這正是 TRIO.BAS 在藥廠與生技產業 QA 與 GMP 環境中的核心價值所在。
如欲進一步了解相關產品,歡迎與 爾榜燈生技 聯繫,我們將提供完整且專業的技術支援。




